
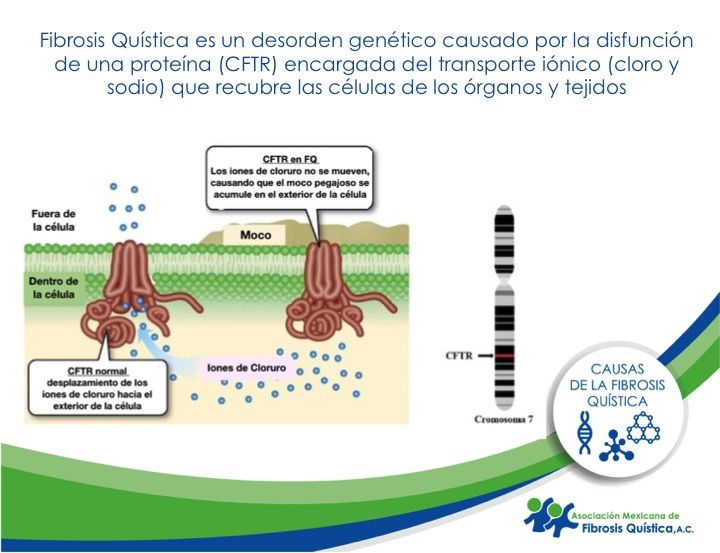
Fibrosis Quística (FQ) una enfermedad hereditaria, congénita y crónica, ocasionada por mutaciones de un gen que transcribe para una proteína conocida como CFTR las cual funciona como un canal de sales y agua. Por lo tanto, FQ es resultado de una alteración genética en el transporte de agua y sales en las células que recubren los distintos órganos y tejidos, principalmente el aparato respiratorio y digestivo, provocando un moco anormalmente pegajoso que; Bloquea los conductos respiratorios y proporciona un medio ambiente ideal para el desarrollo de infecciones.
Bloquea el flujo hacia el intestino de enzimas pancreáticas, necesarias para la digestión normal de los alimentos.
En 1950 la edad promedio de un niño con FQ era de 4 años, hoy gracias a los avances de la ciencia, el 27% de los pacientes con FQ en México alcanzan la vida adulta. A pesar de considerarse una enfermedad crónica hoy se tiene la esperanza de un tratamiento definitivo la cual sin un tratamiento adecuado provoca la muerte durante la infancia o adolescencia.
El diagnóstico temprano y un tratamiento oportuno se traducen en más y mejores expectativas de vida.

CFTR es una proteína que se encuentran en las membranas de las células de los tejidos (secreciones exocrinas). Su principal función consiste en facilitar el transporte activo de iones de cloro hacia el exterior de la célula, así como introducir sodio y agua. En FQ el gene que codifica la proteína CFTR presenta una mutación, lo cual ocasiona que la concentración de cloro y sodio en las secreciones corporales este aumentada.
Cerca de 1.400 mutaciones del gene CFTR se han descrito y se encuentran registradas en Cystic Fibrosis Mutation Database, dentro de estas mutaciones la más frecuente es la DF508, Esta mutación está presente en 70% de los cromosomas FQ en población caucásica y su frecuencia en pacientes mexicanos en menor (aproximadamente 40%).

Fibrosis quística o FQ es un trastorno genético que afecta los pulmones, pero eso es solo una parte de la historia, de hecho, el nombre de fibrosis quística se refiere a los efectos de la enfermedad en el páncreas, donde puede conducir a quistes que son sacos llenos de agua envueltos en una membrana y fibrosis que es la formación de tejido fibroso (cicatrices) que puede reemplazar o infiltrar tejido normal en un órgano.
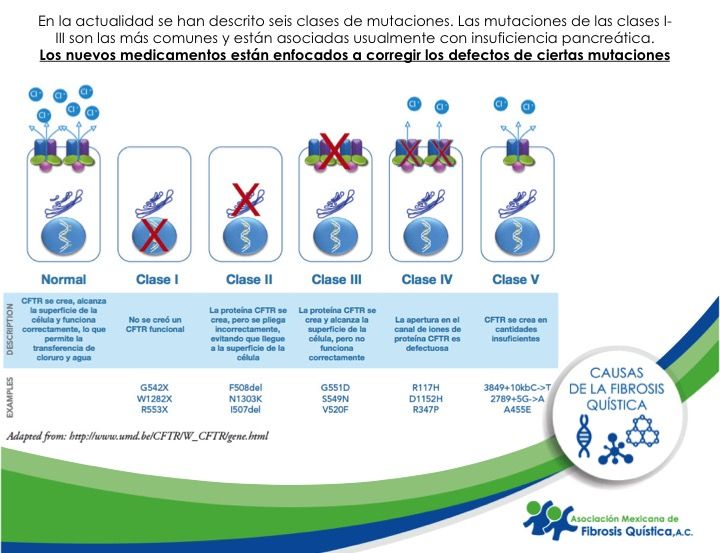
Clasificación de las mutaciones:
En la actualidad se han descrito seis clases funcionales de mutaciones. Las mutaciones de las clases I a III, corresponden a mutaciones graves y son las más comunes (95%), están asociadas usualmente con insuficiencia pancreática.
Clase I: mutaciones que alteran la producción de la proteína.
Se deben a un defecto en la producción de la proteína CFTR en el núcleo de la célula, lo cual provoca su degradación. Estas mutaciones tienen como consecuencia la ausencia total o parcial de la proteína, por lo que el CFTR es completamente disfuncional. Ejemplo de estas mutaciones es la G542X, y todas aquellas cuya terminación es X.
Clase II: mutaciones que alteran el proceso de maduración celular de la proteína.
Ciertas mutaciones alteran la maduración de la proteína y su transporte a la membrana de la célula, de manera que el CFTR no está presente en la membrana o lo está en muy baja cantidad. El resultado es un CFTR defectuoso que se destruye durante su maduración en la célula.
Estas variaciones son las más frecuentes ya que incluyen la mutación DF508.
Clase III: mutaciones que alteran la regulación del canal de Cl-.
La proteína CFTR está compuesta dominios que proporcionan energía, otros que ayudan a anclarlo en la membrana de la célula y otros que actúan como compuerta, permitiendo la salida del cloro. Las mutaciones clase funcional III, afectan el dominio que proporciona la energía al CFTR, lo cual reduce su eficiencia para el intercambio de cloro y sodio, es decir hay una falla en la apertura de la compuerta del CFTR. Un ejemplo son las mutaciones G511D y S549N.
Clase IV: mutaciones que alteran la conducción a través del canal de cloro.
Estas mutaciones afectan el anclaje o sostén del CFTR en la membrana de la célula y por lo tanto producen un CFTR inestable, provocando una disminución del flujo del cloro. Como ejemplo podemos resaltar la mutación R117H.
Clase V: mutaciones que alteran la estabilidad del ADN.
Suelen ser mutaciones el alteran el paso en la transcripción del ADN hacia el ARN mensajero dentro del núcleo de la célula, permitiendo cierta cantidad de CFTR funcional. Un ejemplo es la mutación A455E.
Clase VI: mutaciones que alteran la estabilidad de la proteína CFTR madura.
Conllevan un funcionamiento relativamente normal del CFTR en la superficie de las células para un intercambio de cloro y sodio.
Todas las mutaciones del gene CFTR pertenecen a una de estas clases funcionales, ello resultante importante ya que sienta las bases de la investigación actual con el descubrimiento de nuevos medicamentos que actúan como modificadores del CFTR, los cuales actúan sobre cada una de las clases funcionales.
Es necesario recordar que una persona tiene FQ porque recibió un gene CFTR (mutación) de mama y uno de papa, es decir 2 genes CFTR o mutaciones, que pueden ser la misma o diferente. Cuando una persona con FQ tiene dos mutaciones graves (clase funcional I, II o III), tendrá síntomas más graves que si tiene una mutación clase funcional I, II o III y la otra mutación es clase funcional IV, V o VI, en cuyo caso los síntomas serán leves, 2 mutaciones de la clase funcional IV, V o VI no dan síntomas relacionados con FQ.
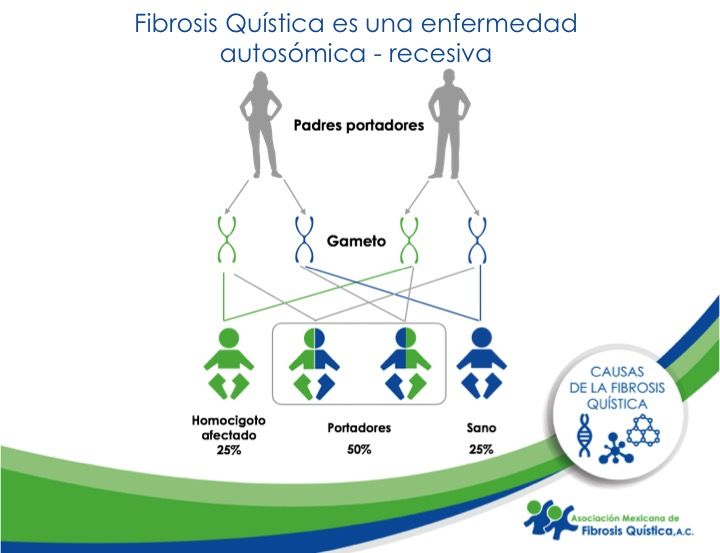
Si un rasgo, trastorno o enfermedad es autosómico recesivo, significa que un individuo debe recibir el Gameto mutado de ambos padres para heredar el rasgo, trastorno o enfermedad
– Se afectan por igual a hombres y mujeres.
– Como regla, si un padre tiene FQ y el otro no y no es portador, ninguno de los descendientes hereda la enfermedad, pero todos serán portadores.
– Si un padre tiene FQ y el otro no pero es portador, existe un 50% de probabilidad de que un descendiente tenga FQ, y los restantes resultan portadores pero sin heredar la enfermedad.
– Entre dos individuos portadores, existe un 25% de probabilidad de que un descendiente se encuentre afectado (FQ), un 50% de que resulten portadores pero sin manifestar la afección, y un 25% de probabilidad de no presentar ningún alelo recesivo (sano).
Ver más slideshows:





Mi niño tiene fibrosos quistica
Hola Laura! Estamos aqui para apoyarte. Avísanos si requieres alguna información en especifica.
Buenos días. Quería saber que repercusiones tiene un paciente con dos mutaciones tipo IV muchas gracias
Buenas noches mi niño tiene 4 años acaba de ser diagnósticado con F.Q. me gustaría acercarme a ustedes pero no se que tan costoso sería y como es el procedimiento para concertar una cita con ustedes !!